La destilación es una técnica de separación que se utiliza para extraer una mezcla sólida en un líquido. Es básicamente el proceso de calentar el líquido para formar vapores y luego condensar los vapores para recuperar el líquido. El líquido que se obtiene al realizar la condensación del vapor se denomina destilado. Los líquidos miscibles se mezclan para formar una solución, por ejemplo, una mezcla de etanol y agua. Los líquidos inmiscibles no se mezclan bien. Por ejemplo, aceite y agua. Los dos líquidos que son miscibles entre sí en todas las proporciones se pueden denominar como una mezcla binaria de líquido. Esta técnica se utiliza para la segregación de componentes de una mezcla de dos líquidos miscibles con suficiente diferencia de puntos de ebullición (BP), que pueden hervirse sin sufrir descomposición.
La destilación es preferible cuando tanto el sólido como el líquido deben extraerse de la solución. También conocida como destilación simple, se basa en las diferencias observadas en la volatilidad y las correspondientes presiones de vapor observadas en los componentes de una mezcla.
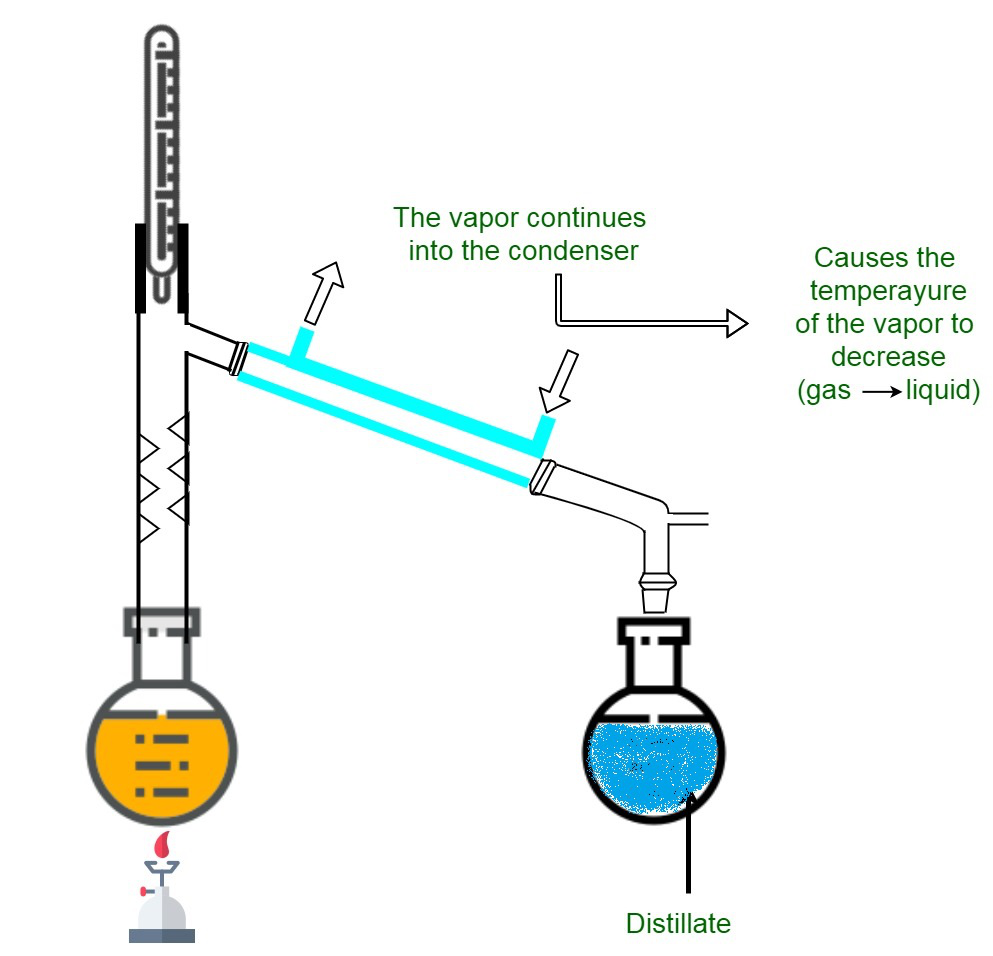
Proceso de destilación
- Una mezcla homogénea que contiene un sólido y un líquido se calientan juntos en un matraz de destilación cerrado.
- El líquido escapa formando vapores ya que son volátiles.
- Estos vapores se enfrían haciéndolos pasar por el condensador.
- Se obtiene líquido puro por condensación en el recipiente tomado.
- El sólido no volátil se deja como residuo.
Equipo necesario para la destilación
El proceso de destilación utiliza básicamente el siguiente aparato:
- Destilador : Se utiliza una cámara de vaporización para colocar el material a destilar. Se calienta para proporcionar la vaporización de los componentes volátiles. También está conectado a un condensador y se fija una trampa en el medio.
- Condensador: Se utiliza para condensar el vapor. Se mantiene frío haciendo circular agua/aire a través de la chaqueta. Los condensadores están disponibles como condensadores de una sola superficie, condensadores de múltiples superficies.
- Recipiente: Se utiliza para recolectar el destilado.
Principio de destilación
- La destilación se lleva a cabo en los puntos de ebullición del disolvente. La ebullición tiene lugar cuando la presión de vapor es equivalente a la presión atmosférica.
- La separación de los componentes de la mezcla se produce mejor en caso de mayor volatilidad relativa de un líquido.
- Al suministrar calor al líquido, el vapor hierve y luego se produce la condensación.
Destilación fraccionada
La destilación fraccionada se utiliza para separar líquidos miscibles que son volátiles por naturaleza. Los puntos de ebullición de estos líquidos están lo suficientemente cerca. El aparato de columna de fraccionamiento se utiliza para simular la separación. También conocido como rectificación, ya que el vapor se condensa parcialmente y se devuelve como líquido. Básicamente es un proceso en el que la vaporización de una mezcla líquida da lugar a una mezcla de constituyentes, seguida de la extracción del componente requerido en su forma pura.
Sin embargo, esta técnica solo se puede utilizar para separar líquidos miscibles, que forman mezclas azeotrópicas PURA.
Principio:
- Al destilar la mezcla líquida, se produce la condensación parcial del vapor en una columna de fraccionamiento.
- En la columna, el vapor que avanza del alambique entra en contacto con el vapor de condensación que regresa al alambique. Esto provoca el enriquecimiento del vapor con el componente más volátil.
- Mediante la condensación constante y el calentamiento del vapor, se logra un equilibrio entre el líquido y el vapor. Esto da como resultado la extracción de un componente más volátil de la mezcla.
Aplicaciones de la Destilación Fraccionada:
La destilación fraccionada se puede utilizar para separar las mezclas como:
- Acetona y agua
- cloroformo y benceno
- Separación de gases del aire.
Embudo de separación
La técnica utilizada para la separación de dos líquidos inmiscibles se realiza mediante un aparato llamado embudo de separación. Es un tipo especial de embudo que tiene una llave de paso en su vástago que permite o detiene el flujo de un líquido desde él. La separación de dos líquidos inmiscibles por un embudo de separación depende de las diferencias en las densidades de los líquidos que los componen. El líquido más pesado se deposita en el fondo y el líquido más liviano permanece como una capa superior.
Aplicaciones del embudo de decantación:
- Agua y queroseno
- Petróleo y agua
Aplicaciones de la destilación:
- Purificación de disolventes orgánicos-alcohol absoluto (100%).
- Separación de sustancias no volátiles de las volátiles.
- Purificación de fármacos fabricados mediante el proceso químico.
- Refinación de productos petrolíferos- Éter de petróleo 60,80.
- Recuperación de disolventes- síntesis.
- Retire la sal del agua para preparar agua potable.
- Metanol o etanol del agua
- La concentración de aceites y bebidas en la industria alimentaria.
Ejemplos de preguntas
Pregunta 1. ¿Diferenciar entre destilación simple y destilación fraccionada?
Responder:
|
Destilación Simple |
Destilación fraccionada |
| El vapor pasa directamente a través del condensador. | El vapor debe pasar a través de una columna de fraccionamiento en la que se produce una condensación parcial del vapor. |
| El condensado se recoge directamente en el receptor. | La condensación se produce en la columna de fraccionamiento, lo que hace que una parte del vapor de condensación vuelva al alambique. |
Pregunta 2. ¿Es posible purificar completamente una mezcla sobre la base de la destilación?
Responder:
Cualquier componente de la mezcla no puede tener presión parcial cero. Como resultado de esto, no se puede obtener una muestra completamente pura de un componente de una mezcla. Sin embargo, se pueden obtener muestras de alta pureza si alguno de los componentes de la mezcla tiene una presión parcial cuyo valor es cercano a cero.
Pregunta 3. Muestre experimentalmente que el agua de mar contiene sal.
Solución:
Se puede probar con la ayuda de la destilación que el agua de mar contiene sal. Cuando se hierve el agua de mar, las moléculas de agua que contiene se evaporan de la superficie en forma de vapor. Luego se condensan en la parte más fría del vaso de precipitados. Como resultado de esto, se produce toda la evaporación del agua, dejando solo la sal como residuo.
Pregunta 4. ¿Cómo ayudan las obstrucciones en una columna de fraccionamiento en la destilación fraccionada?
Responder:
En la destilación fraccionada, la separación de los componentes se produce en función de su punto de ebullición. Estas obstrucciones ayudan en la disposición de las sustancias en el orden en que las sustancias que tienen un punto de ebullición más bajo estarán en la parte superior mientras que las sustancias con un punto de ebullición más alto estarán en la parte inferior.
Pregunta 5. ¿Qué sucede al aumentar la presión en una columna de destilación?
Responder:
- La eficiencia de la destilación disminuirá.
- La volatilidad relativa disminuirá.
- La relación de reflujo será mayor.
- La curva de equilibrio se contrae en mayor medida hacia la línea diagonal.
Pregunta 6. ¿Cuáles son las limitaciones bajo las cuales se debe realizar el proceso de destilación simple?
Responder:
Se puede realizar una destilación simple para:
- Sustancia pura o “casi pura”. Cualquier sustancia con menos del 10% de impurezas se considera pura.
- Una mezcla donde los puntos de ebullición de las impurezas son muy altos,
- Mezcla con una gran diferencia entre los puntos de ebullición de los constituyentes.
Pregunta 7. Explique la naturaleza del residuo en el fondo del matraz.
Responder:
El proceso de destilación se realiza por la mezcla de líquidos que tienen una diferencia suficiente en sus correspondientes puntos de ebullición. Por lo tanto, el residuo en la parte inferior del flash debe ser de naturaleza no volátil.
Publicación traducida automáticamente
Artículo escrito por yashkumar0457 y traducido por Barcelona Geeks. The original can be accessed here. Licence: CCBY-SA