En nuestro entorno, nos encontramos con cosas que son diferentes en forma, tamaño, altura, estructura y textura. Según los científicos, todo en este universo está hecho de un material llamado ‘materia’. Podemos ver que la materia ocupa algo de espacio y masa, de otra manera podemos decir que la materia tiene algo de ‘volumen’ y ‘masa’. Sin embargo, en la antigüedad no había ninguna pista para los científicos, por lo tanto, en ese momento, los filósofos indios creían que todo en este universo, ya sea vivo o no vivo, se puede dividir en ‘panch tattvas, es decir, aire, agua, fuego, cielo y tierra .
Ahora, en este artículo, discutiremos sobre la materia, sus propiedades físicas sobre la base de su clasificación y también estudiaremos sus tipos, es decir, sólido, líquido y gas en breve.
¿Que sucede?
La materia se refiere a las cosas materiales que nos rodean que tienen masa, espacio ocupado y su presencia puede ser sentida por uno o más de nuestros cinco sentidos. Todo en este universo está hecho de material que los científicos han llamado ‘materia’.
Por ejemplo, el agua, el aire, las estrellas, las plantas, una pequeña gota de agua o incluso una pequeña partícula de arena son materia, pero las emociones como el amor, el odio, el dolor, etc. son sentimientos pero no importan.
La materia es cualquier cosa que ocupa espacio y tiene masa.
Espacio: El espacio ocupado por una sustancia se conoce como ‘volumen’.
Masa: La cantidad de metal presente en un objeto se llama su ‘masa’.
Clasificación de la materia
Los primeros filósofos indios clasificaron la materia en forma de 5 elementos básicos como aire, tierra, fuego, cielo y agua llamados ‘ panch tatva’. Los antiguos filósofos griegos también aplicaron una clasificación similar de la materia. Clasificación en base a propiedades físicas y propiedades químicas. Lo que se observa y mide sin cambiar la identidad química de las muestras, como el color, la longitud y el volumen, son propiedades físicas, y lo que se observa y mide que simplemente cambia su identidad química se denomina propiedades químicas.
Según el estado físico de la materia, se clasifica en sólido, líquido y gas. Sobre la base de la composición química, la materia se clasifica como sustancia pura y mezcla. Las sustancias puras pueden ser elementos y compuestos, mientras que las mezclas pueden ser mezclas homogéneas y mezclas heterogéneas.
Naturaleza física de la materia
- Una materia está formada por partículas muy pequeñas que pueden ser átomos o moléculas, por ejemplo, cuando disolvemos una cucharada de sal o azúcar en un vaso de agua.
- La materia está compuesta de partículas : las partículas de materia son muy pequeñas más allá de la imaginación, estas partículas tienen espacio entre ellas.
- Las partículas de materia están en movimiento continuo : esto se debe a que la energía cinética que poseen las partículas aumenta al aumentar la temperatura y, por lo tanto, las partículas se mueven mucho más rápido.
- Las partículas de materia se atraen entre sí por fuerzas de atracción : las fuerzas de atracción unen las partículas de materia en un solo cuerpo y también conducen a la disposición de las partículas. Las partículas de materia tienen una fuerza que actúa entre ellas.
Nota: Tanto el azúcar como la sal se componen de partículas muy pequeñas que se desprenden de cada gránulo de azúcar y desaparecen en el agua al disolverse, es por eso que la solución tiene un sabor dulce, pero las partículas no se pueden ver, esto muestra que el agua tiene suficiente espacio para ajustarse ( disolver) partícula diminuta de azúcar o sal.
Características de las partículas de materia
- Las partículas de materia tienen espacio entre ellas.
- Las partículas de materia se mueven continuamente.
- Poseen algo de energía llamada energía cinética a medida que aumenta la temperatura, la energía cinética de las partículas aumenta y, por lo tanto, las partículas se mueven más rápido.
- Las partículas de materia se atraen entre sí, existe una fuerza de atracción entre las partículas conocida como fuerza de atracción intermolecular.
- La fuerza se llama Fuerza Cohesiva.
Estados de materia
- Sólido: sólido tiene una forma definida y un volumen definido. Por ejemplo, cubitos de hielo y madera.
- Líquido: un líquido tiene un volumen definido pero no una forma definida. Por ejemplo, agua y leche.
- Gas- Ael gas no tiene forma definida ni volumen definido. Por ejemplo, nitrógeno, oxígeno, etc.
- Plasma : el plasma se considera el cuarto estado de la materia. El plasma es una mezcla de electrones e iones libres. Ocurre naturalmente en las estrellas. Dentro de las estrellas, la temperatura es tan alta que los átomos se descomponen. Y, esta mezcla de electrones libres e iones en un estado se llama plasma. El sol y las otras Estrellas brillan debido a la presión del Plasma en ellas. El plasma también se puede hacer en la tierra al pasar electricidad a través de gases a menos temperatura. El plasma hace que el tubo fluorescente brille.
- BE condensado (bose- einstein ) – En 1921, el científico indio Satyendra Nath Bose hizo algunos cálculos para el quinto estado de la materia. Sobre la base de su cálculo, Albert Einstein predijo la existencia de un nuevo estado de la materia. El quinto estado de la materia fue finalmente logrado por tres científicos de Cornell, Kellerie y Wieman de EE. UU., enfriando gas en una densidad extremadamente baja a una temperatura muy baja.
Ahora, estudiemos en detalle las propiedades de los tres estados principales de la materia.
Propiedades del Sólido
- Forma definida, tamaño, volumen y límites definidos.
- Compresibilidad despreciable.
- Los sólidos tienden a mantener su forma cuando se someten a una fuerza exterior.
- Son rígidos, difíciles de cambiar de forma.
- La masa por unidad de volumen de una sustancia se llama densidad .
- La fuerza intermolecular es alta en los sólidos.
- La energía cinética es muy baja en los sólidos.
- Los sólidos no poseen la propiedad de difusión.
- Una banda elástica es sólida porque puede cambiar su forma bajo la fuerza y recuperar su forma cuando se quita la fuerza si se aplica una fuerza excesiva se rompe. Este es un caso excepcional del sólido.
- La sal y el azúcar toman la forma del recipiente en el que se colocan, pero la forma de sus cristales no cambia, por lo que son sólidos.
Propiedades del Líquido
- No tienen una forma definida o límites definidos pero tienen un volumen fijo.
- Se pueden comprimir.
- En Ciencias el nombre común de gases y líquidos es fluido.
- Los líquidos no son rígidos pero tienen la propiedad de fluir, por eso los líquidos se llaman fluidos.
- La fuerza intermolecular es menor que la de los sólidos.
- En líquido la energía cinética es más que sólida.
- El líquido tiene una densidad moderada.
- Los líquidos poseen la propiedad de la difusión.
- Pueden tomar cualquier forma.
- Los gases oxígeno y dirust de carbono de la atmósfera se difunden y disuelven en agua. Debido a estos gases, las plantas y los animales acuáticos pueden sobrevivir.
- La difusión es mucho más en líquido que en sólido debido al libre movimiento de partículas de líquido.
Propiedades del gas
- El gas no tiene una forma definida ni un volumen definido.
- Se pueden comprimir mucho.
- Los gases tienen máxima fluidez y menos rigidez.
- La fuerza de atracción intermolecular es mínima.
- La energía cinética de sus partículas es máxima.
- Los gases no tienen densidad.
- Pueden tomar cualquier forma.
- Difusión muy rápida.
- Las partículas de un gas pueden moverse libremente y, por lo tanto, los gases pueden fluir en cualquier dirección. Ocupan todo el volumen disponible para ellos.
- GLP = Gas Licuado de Petróleo y GNC = Gas Natural Comprimido que es combustible en los vehículos.
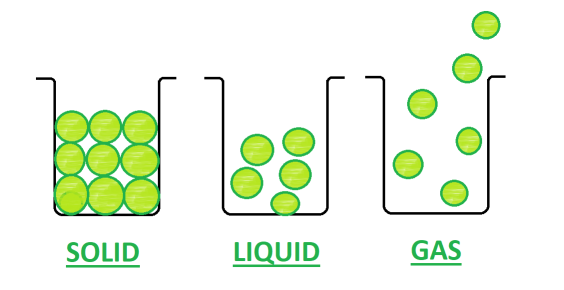
Diferencia entre sólido, líquido y gas
| SÓLIDO | LÍQUIDO | GAS | |
| 1. | Los sólidos tienen un volumen fijo y una forma definida. Tiene límites definidos. | Los líquidos tienen un volumen fijo pero no tienen forma fija. Toman la forma de recipientes pero no lo llenan. | Los gases no tienen forma fija ni volumen fijo. Toman la forma y el volumen de la vasija. Llenan el recipiente. |
| 2. | Los sólidos son rígidos y no son comprimibles. | Al igual que los sólidos, los líquidos no se pueden comprimir mucho. | Los gases son fácilmente comprimibles. |
| 3. | El espacio y el movimiento de una partícula es mínimo. | El movimiento de partículas es intermedio. | El movimiento de partículas es máximo. |
| 4. | Los sólidos no fluyen y no se difunden. | Los líquidos generalmente fluyen fácilmente y pueden difundirse más que los sólidos. | Los gases fluyen fácilmente y tienen una fuerte tendencia a la difusión. |
| 5. | Los sólidos tienen altas densidades. | Generalmente son menos densos que los sólidos. | Los gases tienen densidades muy bajas y son muy ligeros. |
| 6. | Los sólidos se quedan donde se colocan. | Se pueden verter líquidos. | Los gases se esparcen rápidamente. |
| 7. | La fuerza de atracción entre partículas es más fuerte en los sólidos. | Las fuerzas entre partículas son más débiles. | La fuerza de atracción entre partículas es la más débil. |
| 8. | Sólido posee rigidez. | El líquido posee fluidez. | Los gases poseen la mayor fluidez. |
| 9. | Por ejemplo, hielo, madera, azúcar, etc. | Ex- agua, jugo, etc. | Ex- Oxígeno, Nitrógeno, etc. |
Ejemplos de preguntas
Pregunta 1: ¿Qué es la difusión?
Solución:
La mezcla de partículas de dos tipos diferentes de materia por sí solas se llama difusión.
O
La mezcla espontánea de partículas de dos tipos diferentes de materia se llama difusión. La velocidad de difusión se vuelve más rápida con el aumento de la temperatura porque a alta temperatura las partículas tienen más energía y, por lo tanto, se mueven más rápido.
Por ejemplo -aroma de perfume, olor a comida caliente chisporroteante
Pregunta 2: ¿Qué es la fuerza de atracción entre partículas?
Solución:
La materia tiene fuerza de atracción entre partículas. Esta fuerza mantiene unidas a las partículas. Depende de la naturaleza de la materia.
Pregunta 3: ¿Qué tan pequeñas son estas partículas, las partículas de materia?
Solución:
Las partículas de materia son tan pequeñas que ni siquiera podemos verlas a simple vista.
Pregunta 4: ¿Qué sucede cuando se pincha un globo hinchado con un alfiler?
Solución:
Reventará y se producirá la difusión.
Pregunta 5: ¿Cuál es la razón detrás de la observación de que el líquido no se puede comprimir mientras que los gases sí?
Solución:
Esto se debe al fenómeno del espacio intermolecular que es muy grande en los gases, por lo que tienen capacidad para comprimirse, mientras que los líquidos tienen menos espacio intermolecular, por lo que no se pueden comprimir.
Pregunta 6: ¿Por qué los sólidos tienen una forma fija?
Solución:
Los sólidos tienen forma fija porque su fuerza intermolecular es muy fuerte, por eso siempre sostienen una estructura geométrica regular.
Pregunta 7: Ordene las siguientes sustancias en orden decreciente de la fuerza de atracción intermolecular.
- Dirust de carbono
- Azúcar
- Jugo
Solución:
Azúcar > Jugo > Dirust de carbono
Pregunta 8: ¿Qué es el Movimiento Browniano?
Solución:
El movimiento en zigzag de las pequeñas partículas suspendidas en un líquido o gas se denomina movimiento browniano.
Publicación traducida automáticamente
Artículo escrito por kavyagupta0098 y traducido por Barcelona Geeks. The original can be accessed here. Licence: CCBY-SA