Cada vez que visitamos un laboratorio, podemos encontrar una serie de productos químicos guardados allí. Todos estos productos químicos pueden parecernos similares a nosotros, pero no lo son. Algunos de estos pueden ser ácidos, bases o sales. Podemos identificar fácilmente estos productos químicos con la ayuda de las etiquetas de las botellas. Pero, ¿qué sucede si desea saber si una sustancia química es un ácido o una base sin su etiqueta? ¿Alguna vez te has preguntado cómo los científicos identifican los ácidos o las bases en un laboratorio o cómo clasifican el producto de una reacción química como ácido o base? Aquí es donde los indicadores son realmente útiles para nosotros. Discutamos los indicadores en este artículo. Antes de analizar qué son los indicadores y sus tipos, analizaremos qué son los ácidos y las bases:
- Ácidos: en la antigüedad, cualquier cosa que supiera agria se consideraba un ácido. De acuerdo con la definición moderna de un ácido, cualquier compuesto que puede donar un ion de hidrógeno a otra molécula o compuesto es un ácido. En otras palabras, podemos decir que cualquier molécula que pueda desprenderse de un ion H+ y aún exista se sabe que es un ácido. Los ácidos generalmente tienen un sabor agrio y pueden ser ácidos fuertes o ácidos débiles.
- Bases: En la antigüedad, cualquier cosa que tuviera un sabor amargo se consideraba una base. De acuerdo con la definición moderna de la base, se dice que cualquier compuesto que puede aceptar un ion de hidrógeno cedido por un ácido es una base. En otras palabras, podemos decir que cualquier molécula que puede aceptar un ion H+ de un ácido y aún existir se conoce como base.
Las bases solubles en agua se denominan álcalis. Los ácidos y las bases reaccionan entre sí para dar lugar a sal y agua. Esta reacción se denomina reacción de neutralización .
Ácido+Base → Sal+Agua
p.ej
HCl (Ácido) + NaOH (Base) → NaCl (Sal) + H 2 O (Agua)
¿Qué son los Indicadores Químicos?
Los indicadores son ácidos débiles o bases débiles que muestran un cambio de color a medida que cambia la concentración de iones de hidrógeno en una solución o cambia el pH de una solución. Los indicadores se disocian ligeramente en el agua para formar iones.
Algunos ejemplos de indicadores son el tornasol, la cúrcuma, la fenolftaleína, etc.
Cualquier material que ofrezca una evidencia visual de la presencia o ausencia de un umbral de concentración de una especie química, como un ácido o un álcali en una solución, generalmente por un cambio de color, se denomina indicador químico. Un químico llamado amarillo de metilo, por ejemplo, le da a una solución alcalina un color amarillo. Cuando se agrega ácido gradualmente, la solución permanece amarilla hasta que se neutraliza todo el álcali, momento en el cual se vuelve roja.
Tipos de indicadores
Los indicadores son principalmente de dos tipos:
- Indicadores naturales: Los indicadores que ocurren naturalmente en el medio ambiente se denominan indicadores naturales. por ejemplo, tornasol, cúrcuma, etc.
- Indicadores Artificiales: Son indicadores artificiales aquellos indicadores que se obtienen mediante alguna reacción química pero no de forma natural o se preparan artificialmente en el laboratorio. por ejemplo, fenolftaleína, naranja de metilo, etc.
- Indicadores olfativos: Estos son aquellos indicadores que no muestran un cambio de color sino un cambio de olor cuando se agregan a un ácido o una base. Así, los indicadores olfativos son aquellos indicadores cuyo olor cambia según la naturaleza del medio, ya sea ácido o básico.
Indicadores Naturales
El indicador natural es un tipo de indicador que se puede encontrar en la naturaleza y se puede utilizar para detectar si un material es ácido o básico. Repollo rojo, cúrcuma, jugo de uva, cáscara de nabo, curry en polvo, cerezas, remolacha, cebolla, tomate y otras indicaciones naturales son ejemplos.
Las hortensias, por ejemplo, pueden decirte si el suelo es ácido o básico. Si el suelo es ácido, las flores se vuelven azules, moradas si el suelo es neutro y rosas si el suelo es básico. La intensidad del color está determinada por la cantidad de ácido o base en el suelo. Las flores de color azul intenso florecen en suelos extremadamente ácidos, mientras que las flores de color rosa intenso florecen en suelos fuertemente básicos.
Los siguientes son algunos indicadores naturales que se usan comúnmente:
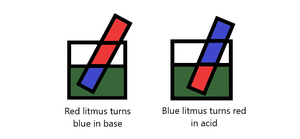
- Tornasol: El tornasol se obtiene de los líquenes y es una mezcla de colorantes solubles en agua que se obtienen de los líquenes. El tornasol generalmente se convierte en un tinte soluble y luego se absorbe en un papel que luego se llama papel de tornasol. El color natural del tornasol es el morado. El tornasol se puede usar para probar si un compuesto es un ácido o una base. Un papel de tornasol rojo se vuelve azul en una solución básica y no muestra ningún cambio de color en soluciones ácidas. Un papel de tornasol azul se vuelve rojo en una solución ácida y no muestra cambio de color en una solución básica. El tornasol neutro se vuelve rojo y azul en soluciones ácidas y básicas respectivamente.
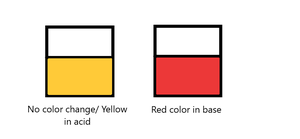
- Cúrcuma: La cúrcuma es un indicador natural y se conoce comúnmente como Haldi. Es de color amarillo brillante. La pasta de cúrcuma se puede usar para probar ácidos o bases. En medio ácido, la cúrcuma es de color amarillo y no muestra ningún cambio de color mientras que en una solución básica su color se torna rojo.
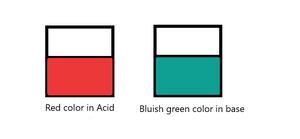
- Indicador de repollo rojo: el repollo rojo se usa comúnmente como verdura, pero su extracto también se puede usar como indicador. El repollo rojo es un indicador natural. El repollo rojo contiene un pigmento antocianina que es responsable del cambio de color del repollo rojo en un ácido o base. El extracto de col roja se utiliza como indicador. El repollo rojo tiene un color morado intenso de forma natural. El extracto de col lombarda se vuelve rojo en medio ácido con pH < 7 y verde azulado en medio alcalino o básico con pH > 7.
Indicadores artificiales (o sintéticos)
Los indicadores sintéticos, a menudo conocidos como indicadores artificiales, son indicadores de base ácida que se fabrican con productos químicos artificiales.
Los siguientes son algunos indicadores artificiales o sintéticos que se analizan a continuación:
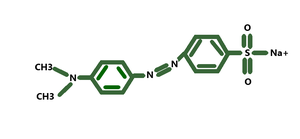
- Naranja de metilo: El naranja de metilo también es un indicador y muestra cambios de color en ácidos y bases. Originalmente es de color naranja. El naranja de metilo sólo se puede utilizar en el caso de ácidos minerales y bases fuertes. No puede identificar ácidos débiles o bases débiles. En un medio ácido, el naranja de metilo se vuelve rojo, mientras que en un medio básico se vuelve amarillo. La estructura del naranja de metilo es como se muestra a continuación:
- Fenolftaleína: La fenolftaleína es un tinte soluble en agua y es de color púrpura oscuro. Se utiliza en forma de solución para probar ácidos y bases. En medio ácido se vuelve incoloro mientras que en medio básico se torna rosa claro. Se utiliza principalmente en valoraciones ácido-base. El color de la fenolftaleína se muestra a continuación en medio ácido y básico:

¿Qué son los Indicadores Universales?
Los indicadores comunes pueden o no mostrar un cambio de color en un amplio rango de pH, pero solo para un pequeño rango. Esto hace que sea difícil identificar los ácidos o las bases. Este problema se resuelve con indicadores universales. Se mezclan varios indicadores para formar un indicador universal que cambia de color en una amplia gama de valores de pH.
Indicadores olfativos:
Un indicador olfativo es una sustancia química que cambia de olor dependiendo de si se combina con una solución ácida o básica. En el laboratorio, los indicadores olfativos se pueden usar para determinar si una solución es básica o ácida, una técnica conocida como titulación olfativa. Definidos de manera simple, los marcadores olfativos son compuestos en soluciones ácidas y básicas que tienen olores distintivos. Por ejemplo, el extracto de vainilla, la cebolla y el aceite de clavo, etc., tienen aromas distintos. Los indicadores olfativos son muy útiles para identificar ácidos o bases para estudiantes con discapacidad visual.
Algunos de los indicadores olfativos son los siguientes:
- Extracto de cebolla: el extracto de cebolla se puede obtener hirviendo el agua y agregando cebolla picada. Cuando el agua se enfría, el extracto de cebolla está listo. El extracto de cebolla muestra el cambio de olor en ácido y bases. Cuando se agrega a un ácido, conserva su olor acre, pero en las bases se vuelve completamente iNodero.
- Extracto de vainilla: el extracto de vainilla funciona igual que el extracto de cebolla. Conserva su olor agradable en una solución ácida pero pierde su olor en un medio básico.
A continuación se presenta la lista de los indicadores y sus colores en ácidos y bases respectivamente:
|
Indicador |
Color en ácido |
Color en Base |
|
naranja de metilo |
Rojo |
Amarillo |
|
fenolftaleína |
Incoloro |
Rosado |
|
Tornasol |
Rojo |
Azul |
|
Cúrcuma |
Ningún cambio |
Marrón rojizo |
|
Extracto de col roja |
Rojo |
Verde azulado |
|
extracto de cebolla |
Sin cambio de color conserva su olor |
Sin cambio de color Se vuelve iNodero |
|
Extracto de vainilla |
Sin cambio de color Conserva su agradable olor. |
Sin cambio de color Pierde su olor |
Importancia de los Indicadores
La naturaleza de un material es significativa en biología, química, ingeniería civil, purificación de agua, agricultura, silvicultura, ciencia de los alimentos, ciencia ambiental, tratamiento de agua, oceanografía, medicina, nutrición y agronomía, entre otros campos.
Los líquenes incluso se utilizan para hacer tornasol. Es una combinación de colores que se disuelve en agua. Luego se absorbe en papel de filtro para crear uno de los primeros tipos de indicador de pH, que se utiliza para determinar la acidez o basicidad de las cosas.
Ejemplos de preguntas
Pregunta 1: ¿Qué quiere decir con un indicador?
Responder:
Un indicador es generalmente un ácido débil o una base débil que se disocia en una solución para formar iones. Los indicadores se utilizan para comprobar si un medio es de naturaleza ácida o básica.
Pregunta 2: Un indicador se volvió rojo en HCl y azul en solución de NaOH. Identifique el indicador.
Responder:
Sabemos que el HCl es de naturaleza ácida y el NaOH es de naturaleza básica. Como el indicador se volvió rojo en ácido y azul en base, seguramente es tornasol.
Pregunta 3: ¿A qué te refieres con indicadores olfativos? Dar ejemplos.
Responder:
Aquellos indicadores que cambian su olor dependiendo de la naturaleza ácida o básica del medio se denominan indicadores olfativos. Ejemplo: extracto de cebolla, extracto de vainilla
Pregunta 4: El repollo rojo se volvió rojo en una solución, mientras que el tornasol rojo no mostró ningún cambio de color. Identificar la naturaleza de la solución.
Responder:
Como el repollo rojo se puso rojo y el tornasol rojo no cambió de color en la solución, la solución debe ser de naturaleza ácida.
Pregunta 5: Los vapores de HCl se pasaron sobre un papel tornasol azul pero no mostró ningún cambio de color. Explique.
Responder:
Como sabemos, los indicadores muestran un cambio de color cuando el ácido o la base se disocian en iones de hidrógeno o hidrrust. Aquí, el HCl se convirtió en vapor y no se disoció en iones, por lo que el papel tornasol no mostró ningún cambio de color.
Pregunta 6: Se lavó con jabón una mancha de cúrcuma y luego se frotó con limón. Identifica los cambios de color.
Responder:
Cuando la mancha de cúrcuma se frota con jabón, se vuelve de color marrón rojizo, pero vuelve a cambiar a su color amarillo original cuando se frota con limón.